卵巢癌發病率位於女性生殖系統惡性腫瘤第3位,致死率居婦科惡性腫瘤之首[1],全世界每年有31.4萬例病例和20.7萬例死亡[2]。約70%的患者在初診時已進展至晚期,5年生存率不足40%。目前卵巢癌從疾病篩查到綜合治療,從多學科協作到疾病全程管理都面臨著一定的挑戰,如何能使卵巢癌患者延長生命週期、提高生活質量從而最大獲益是醫療工作者所共同追求的目標。因此《醫師報》特別邀請寧波大學附屬第一醫院管玉濤教授、浙江大學醫學院附屬二院周建維教授、浙江省人民醫院壽華鋒教授、浙江大學附屬婦產科醫院張松法教授和、江省腫瘤醫院張英麗教授共同深入交流卵巢癌篩查和綜合治療相關臨床經驗及建議。
1
管玉濤教授:卵巢癌早期篩查面臨挑戰,新型標誌物有望提高篩查效率
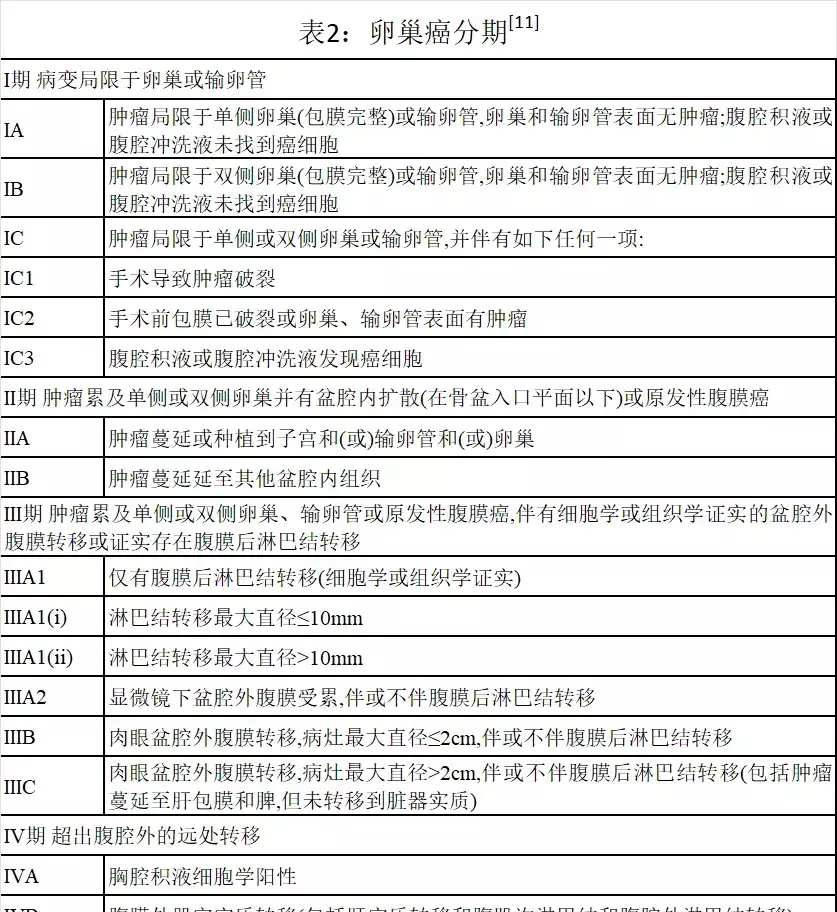
卵巢癌早期診斷可為患者帶來生存優勢,即使是侵襲性高級別、低分化或未分化腫瘤,在I/II期診斷時,其5年生存率高達74%,與III/IV期患者27%的5年生存率相比大大提高[3],因此卵巢癌的早期篩查診斷尤為重要。但是目前卵巢癌的早期篩查面臨諸多難點。首先,卵巢的體積較小且位於盆腔深處,其解剖學特點使其早期病變不易被察覺,加之許多侵襲性卵巢癌起源於輸卵管上皮細胞,本身即具有不容易成像的特點,這些特點均導致了卵巢癌影像學檢查遺漏和誤診的機率較大。其次,卵巢腫瘤缺乏特異性標誌物,炎症或者其他器官腫瘤均可以導致相應腫瘤標誌物的升高;同時,卵巢癌是所有人體腫瘤中型別最多、組織成份最複雜的腫瘤,這一特點也使得並非所有卵巢癌亞型均可透過腫瘤標誌物進行篩查。
卵巢癌目前缺乏早期有效的篩查,但並非意味不進行篩查。尤其對於卵巢癌高危人群,特別是有卵巢癌家族史或BRCA1和BRCA2陽性人群,建議每6個月進行一次超聲檢查和血清CA125 檢查[4],也可在此基礎上聯合其他腫瘤標誌物如HE4進行篩查,以增加卵巢上皮性腫瘤的檢出率。目前,全球正在研究幾種新的生物標誌物和篩選策略,並可能在未來帶來希望。包括DNA甲基化生物標誌物、遊離DNA、迴圈腫瘤DNA(ctDNA)、糖基化Ca125、Olink生物標誌物、以及多癌種早期檢測(MCED)生物標誌物策略[2]。新的標誌物的探索研究有望在尋求有效的卵巢癌篩查策略方面取得巨大進展。
2
周建維教授:卵巢癌篩查方法侷限性與獲益性並存,影像學、血清、基因三管齊下
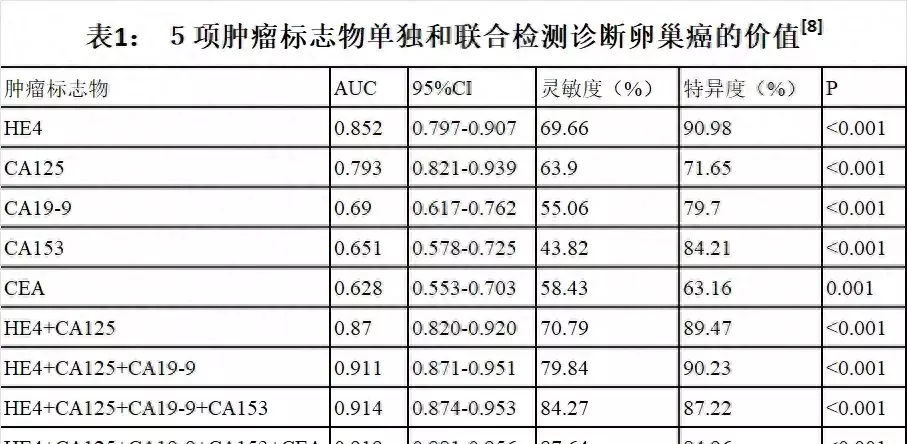
卵巢癌早期的篩查十分困難,到目前為止並沒有較為有效的早篩方法,因此約70%的卵巢癌發現時已到達晚期。但假如能早期篩查出卵巢癌將對患者的治療提供較大的幫助,使患者顯著獲益並長期生存,因此卵巢癌的篩查仍具有一定的必要性。目前對卵巢癌的篩查最常見的方法就是B超[5],B超可以提供有關卵巢形態、血管和內部特徵資訊,在區分良惡性卵巢腫瘤時有較高的敏感性和特異性,若卵巢包塊實性成分居多且血流豐富,則提示包塊惡性的可能性較大。其次是CT和核磁共振[6],CT對於判斷卵巢腫塊的是否實性或者囊實性也有幫助;增強核磁共振或者與CT檢查相結合,都能夠有助於腫塊性質的確定以及判斷其血流的狀況,從而有助於判斷其良惡性。血液腫瘤標誌物在卵巢癌診斷方面也具有一定價值,不同病理型別的卵巢癌可具有不同的腫瘤標誌物,CA125及HE4是上皮性卵巢癌中應用價值最高的腫瘤標誌物,AFP 、β-HCG、NSE、LDH和CA199可用於卵巢惡性生殖細胞腫瘤的輔助診斷,胃腸道轉移性腫瘤可出現CA199及CEA升高,罕見非妊娠性卵巢絨癌也會出現HCG升高,另外ROMA指數是將CA125和HE4血清值與患者絕經狀態相結合的一個評估模型,可幫助評估卵巢惡性腫瘤的風險。這些腫瘤標誌物都具有一定的診斷卵巢惡性腫瘤的臨床參考意義。但假如能將影像學和血清腫瘤標誌物兩者相結合則能顯著提高卵巢惡性腫瘤診斷的準確率,更加精準地對卵巢癌進行早期篩查。
約20%-25%的上皮性卵巢癌與遺傳因素相關,對於有BRCA基因突變、Lynch綜合徵或者兩個一級親屬以上患有卵巢癌的高危人群,首先要增加其篩查頻率,其次可以在適當年齡段進行預防性輸卵管卵巢切除術,從而降低卵巢癌的發生率。
3
壽華鋒教授:綜合治療,全程管理,使卵巢癌患者最大獲益
規範的綜合性治療和全程管理對於卵巢癌患者的治療以及預後至關重要。即使70%的卵巢癌患者發現時已經是晚期並且預後較差,但是隨著治療手段不斷的跟進,大部分患者的治療效果仍較好。此時,患者面臨最大的風險時疾病復發或者再次進展,因此綜合治療和全程管理尤其重要。綜合治療減少了不同部門之間分工的分割,如手術、化療、放療、生物治療、免疫治療包括支援治療可以一併進行,而非割裂開來。從而能夠根據病人病情特點或者病人的特殊需求進行個體化管理以及更加規範化治療,最終達到提高患者生存質量、延長患者生命週期兩個目的。
此外從人文的角度出發,綜合性治療有助於提高患者的醫從性,當患者病情進展或者復發時,能夠及時規範就醫,避免亂就醫、亂服藥的發生,避免病情延誤,減少不必要的損失,使患者能夠長期獲益。
4
張松法教授:多學科診治經驗豐富,機制評價有待完善
鑑於卵巢癌的特點,即:診斷時大部分患者已經進入晚期、廣泛轉移以及複發率較高,多學科協商診療的模式非常適合這一疾病的管理。從診斷到手術時機選擇到術後併發症處理,以及復發後治療決策問題可以透過多學科診療進行流程化管理。對於如何系統且高效的完成多學科診療,主要有以下兩點:首先是主診醫生全程負責和把控,避免由於醫院科室分工精細導致醫生對患者的病情把控缺失;其次是確保合作科室和支援技術齊全,能夠滿足各種治療手段如手術、化療、放療、生物治療、免疫治療均可進行。對於有特殊需求,如有生育需求的患者也能夠聯合其他科室如生殖科等一併進行相關治療和輔助措施。
對於多學科診療(MDT)的實行仍存在一些難點。首先,在主診醫生全程負責的體系背景下,醫生與患者建立一個良性的或者互相信任的關係是非常重要的,而這往往充滿一定挑戰。其次,多學科團隊機制的建立以及人員配置應保持相對穩固,成員之間彼此能夠充分了解並且治療理念也應較為一致。其三,目前對於MDT機制的考評仍面臨著挑戰,如何推進規範化的MDT討論或者協作,以及如何評價病人診治效果、團隊運轉效果和衛生經濟學效果都是目前亟待解決的問題。
5
張英麗教授:制定個性化的治療,留存患者生育功能
卵巢癌患者能否留存生育功能是需要多方面評估和討論的問題。目前認為對有生育要求的年輕早期卵巢癌患者實施保育治療安全有效,可獲得良好的妊娠結局[9]。但需嚴格掌控留存生育治療的手術指徵。首先,從患者角度出發,應確保患者進行了保生育的手術以後,能夠保證腫瘤的治療效果;其次,應確認患者的年齡、病理型別及手術病理分期。2014 年中華醫學會婦科腫瘤分會制定的《婦科惡性腫瘤留存生育功能臨床診治指南》指出保育治療的篩選標準:①患者年齡<40 歲,渴望生育;②患者對FSS帶來的腫瘤復發風險充分知情;③病理分化程度為高分化;④病理提示病變侷限在一側卵巢,對側卵巢和子宮無異常;⑤腹腔細胞學檢查陰性;⑥“高危區域”(子宮直腸陷凹、結腸側溝、腸繫膜、大網膜和腹膜後淋巴結)探查及多點活檢均陰性;⑦有隨診條件;⑧完成生育後視情況再行子宮及對側附件切除術[10]。在滿足留存生育手術的前提下,選擇安全可行的手術方式並注意術中操作,術後合理輔助化療、科學應用卵巢功能保護藥物及輔助生殖技術,從而使患者長期獲益。